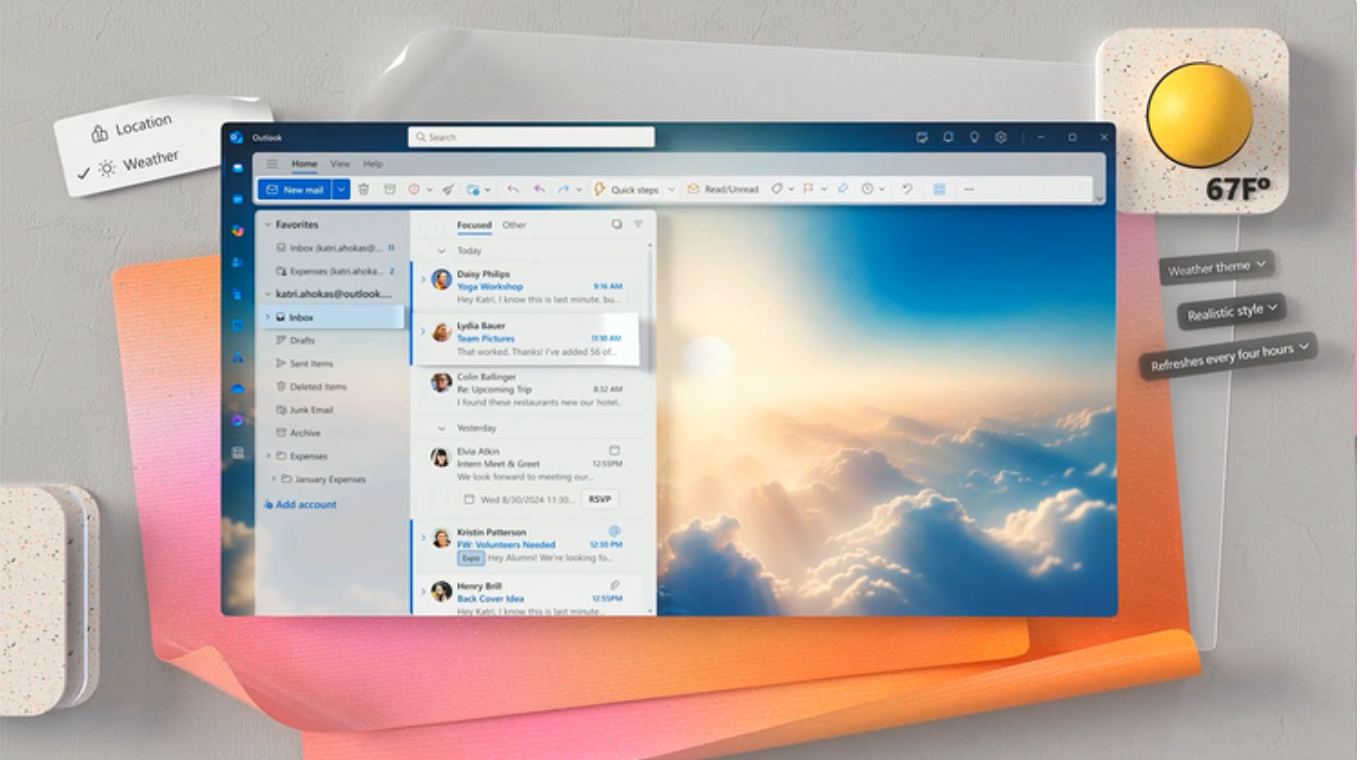
研究人員能夠使用小鼠幹細胞在大鼠體內種植新的胰腺,然後將器官移植到糖尿病小鼠中。
調查結果表明,該技術可以逆轉糖尿病至少在被給予患有糖尿病的藥物的實驗室小鼠中,威脅生命代謝疾病其特徵是無法製造或適當對胰島素做出反應。
在另一物種體內的一個物種的生長器官生長
在另一物種體內種植某種物種的器官的能力也可能鋪平了產生在綿羊或豬等大型動物中生長的可移植人器官的方法。
在實驗中,研究人員將小鼠多能幹細胞植入了經過遺傳工程的大鼠的胚胎中,因此他們不會發展自己的胰腺。多能幹細胞具有發育到體內任何細胞的能力。胰腺的缺失迫使大鼠依靠小鼠細胞發展器官。
小鼠胰腺通常不會被大鼠的免疫系統拒絕,因為在免疫耐受性發展之前,小鼠細胞被注入大鼠胚胎,這是訓練免疫系統以識別其自身組織的時期。
一旦大鼠長大,將胰島素產生的小鼠細胞聚集在一起,將稱為胰島的組聚集在一起,將其移植到糖尿病小鼠中,這些小鼠在遺傳上與形成胰腺的干細胞相匹配。
技術可能會逆轉糖尿病
研究人員發現,糖尿病小鼠使其標準化血糖水平移植後一年多。
小鼠也只需要接受免疫抑製藥物移植後五天,以防止被排斥移植的組織,而不是獲得無與倫比的器官所需的終身免疫抑制治療。在人類中,已知這些藥物具有嚴重的副作用。
移植的胰島包含一些污染的大鼠細胞,這需要使用免疫抑製藥物,但是在移植後五天的治療期間,停止了免疫抑制。
研究人員在他們的書中寫道:“在沒有免疫抑制的情況下,移植的胰島成功地標準化和維持了370天以上的宿主血糖水平(不包括移植後的前5天)。”學習,發表在期刊上自然是1月25日。
“這些數據為異構宿主中胚泡互補產生的PSC衍生胰島的治療潛力提供了原理證明證據。”
可能解決移植患者器官短缺的解決方案
當研究人員在10個月後從一些小鼠中取出胰島時,他們發現小鼠的免疫系統消除了大鼠細胞
斯坦福大學的研究人員Hiromitsu Nakauchi說:“這對於我們希望移植在動物中生長的人體器官的希望是非常有希望的,因為它表明在移植後,患者的免疫系統可以消除任何受污染的動物細胞。”
該研究的發現為減輕移植患者的挽救生命的人體器官短缺提供了希望。