世界上第一種使用的治療方法CRISPR基因編輯技術已被批准。
Exa-cel(也以其品牌Casgevy而聞名)獲得了第一個監管批准2023年11月16日,英國藥物和醫療保健產品監管機構(MHRA)治療兩種使人衰弱的血液疾病:鐮形血球貧血症和輸血依賴性β-核阿無血症。美國食品藥品監督管理局(FDA)隨後批准了該療法作為治療兩個都 疾病。
監管機構批准Casgevy的歷史性決定可能標誌著新時代的開始基因療法。但是,圍繞治療的負擔能力及其長期安全的問題。
這是我們到目前為止對Casgevy的了解。
有關的:青少年收到用CRISPR編輯的新細胞後,她的癌症正在緩解
第一次批准的CRISPR療法是什麼?
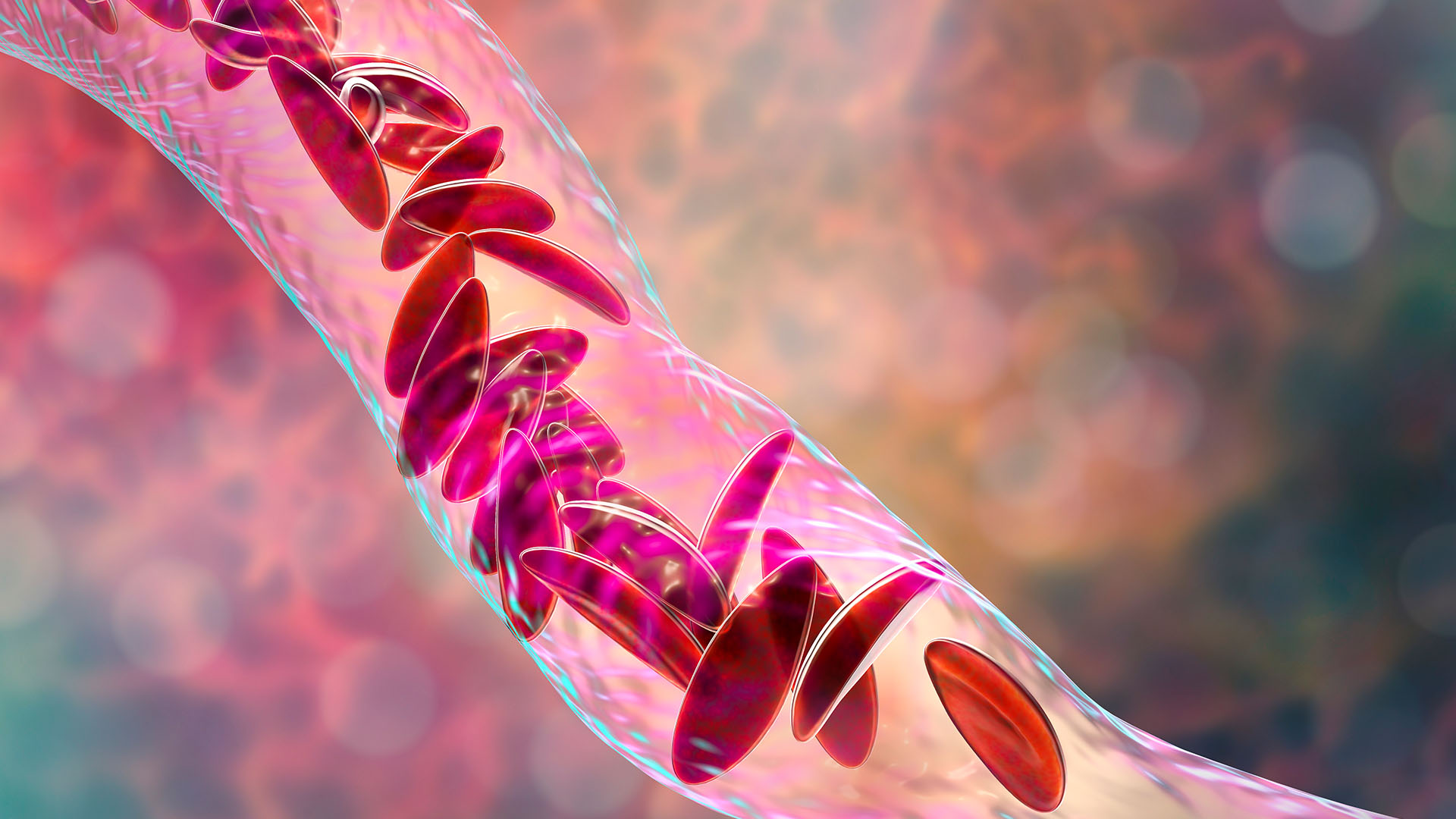
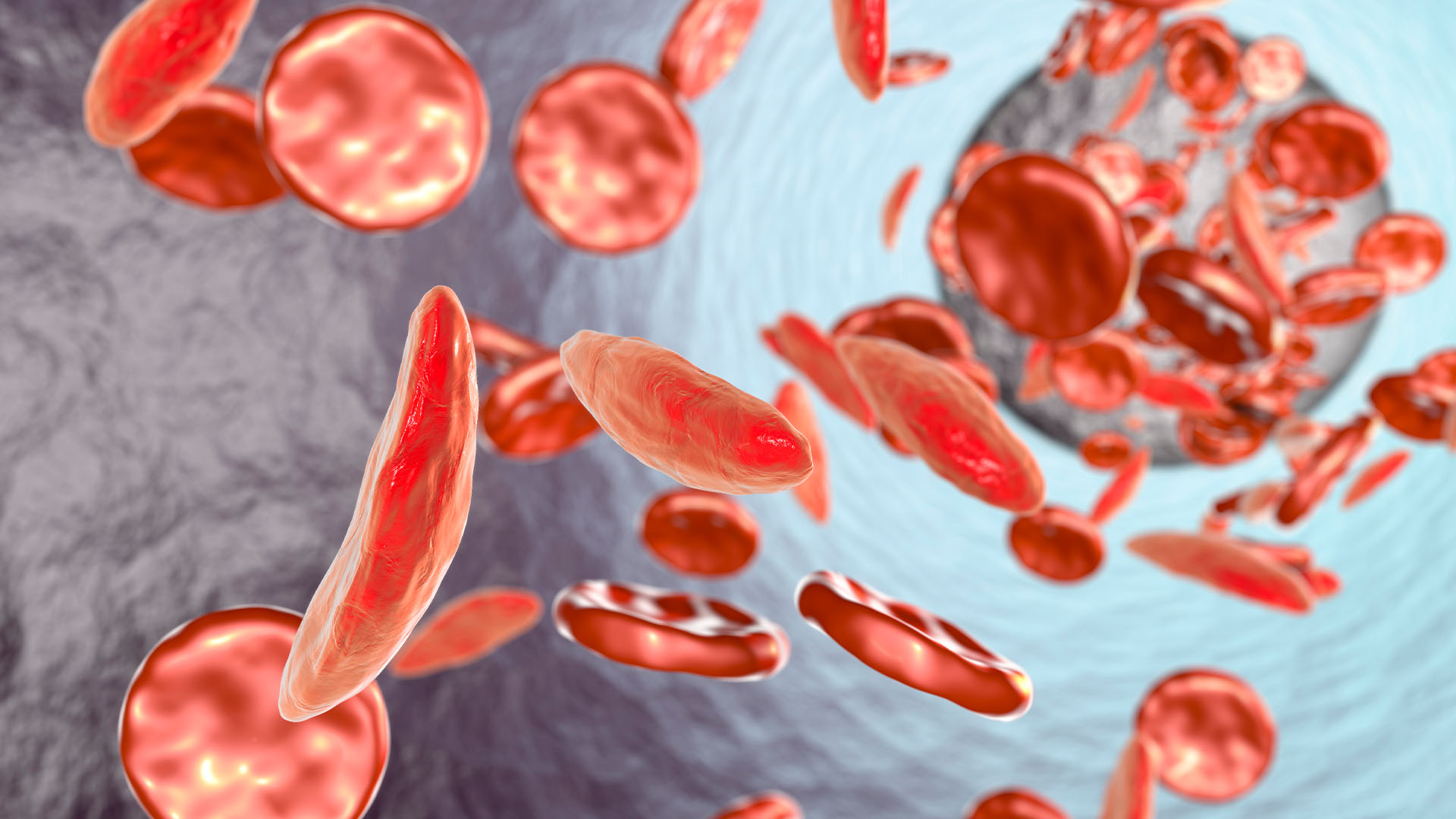
MHRA批准了Casgevy治療鐮狀細胞疾病(SCD)和輸血依賴性β-核阿無血症。這些是終身,是由代碼為血紅蛋白的基因中的突變引起的,這種蛋白質是紅細胞需要在體內轉運氧氣的蛋白質。
超過100,000人據估計,在美國有SCD,但某些人群的速率高於其他人群。例如,每365個黑人嬰兒中有1人出生於SCD。該疾病改變了一個人的紅細胞的形狀,使它們變成C形,而不是圓形。鐮狀細胞迅速死亡,也彼此粘住,阻塞血管。結果,患者發展貧血而且經常經歷劇烈痛苦的回合疼痛危機。
β-地中海貧血會影響周圍100,000人中有1人全球,它不成比例地影響地中海,亞洲,非洲和中東血統。 β-甲性疾病的患者無法產生足夠的血紅蛋白,這會導致嚴重的貧血,而鐮狀細胞性貧血卻是由於缺乏健康的紅細胞。 “依賴輸血”是指該疾病是如此嚴重,以至於患者必須具有常規紅細胞輸血他們一生。
Casgevy如何工作?
Casgevy基於一種革命性的基因編輯技術,稱為CRISPR2012年首次開發。
CRISPR系統使用稱為CAS9的酶從DNA中切出基因。這些“分子剪刀”被引導到靶向DNARNA。該技術是根據一種自然防禦機制改編而來的細菌和其他稱為古細菌對病毒的簡單生物。
casgevy靶向一個稱為的基因Bcl11a。通常會調節的蛋白質的基因代碼從血紅蛋白的胎兒版本切換出生後不久為成人版。但是,在SCD和β-甲性甲性疾病患者中,成年血紅蛋白有缺陷。
Casgevy的目的是禁用BCL11A,從而使人體能夠繼續製作胎兒血紅蛋白,因為成人版本不起作用。為此,造血幹細胞取自患者的骨髓,並在實驗室中使用casgevy編輯Bcl11a基因。然後將具有功能性血紅蛋白的新修飾細胞注入患者的體內。在輸注之前,患者必須服用一種稱為Busulfan的化學療法藥物,以消除仍在其骨髓中的未經編輯的細胞,據統計新聞報導。
調整新編輯的單元的這個過程很長。 MHRA在一家中說:“患者可能需要在醫院設施中至少花一個月的時間,而治療的細胞居住在骨髓中,並開始用穩定的血紅蛋白形式製造紅細胞。”陳述。
在兩項晚期臨床試驗中,Casgevy恢復了大多數SCD和β-甲性疾病患者的血紅蛋白產生,並減輕了症狀。29例SCD患者中有28例接受Casgevy治療後至少一年沒有遇到任何嚴重的疼痛危機。相似地,42例患者中有39名在同一後治療期間,由於β-地中海貧血不需要紅細胞輸血。其餘三名患者需要輸血的可能性降低了70%以上。
Casgevy安全嗎?
儘管有一些短暫的副作用,例如發燒和疲勞,但在兩項後期臨床試驗中,這兩個晚期臨床試驗中的任何一個都沒有嚴重的安全問題。這兩項試驗都是持續的,Casgevy的長期安全性繼續受到MHRA和FDA等監管機構的監控,以及治療療法的製造商,頂點藥物和CRISPR療法。
但是,總的來說,仍然對基於CRISPR的療法的安全存在一些擔憂。也就是說,人們擔心“脫靶”效果,這是在Cas9時發生的作用於基因組的其他部分這不是打算更改並引起不必要的副作用。
“眾所周知,CRISPR會導致虛假的遺傳修飾,對被治療的細胞造成未知後果,”大衛·魯達(David Rueda),倫敦帝國學院的分子和蜂窩生物物理學主席告訴英國科學媒體中心。他說:“在得出結論之前,必須看到這些細胞的全基因組測序數據。”這將涉及對Casgevy編輯的細胞中的所有DNA進行測量,以查看是否存在脫靶效應。
Casgevy在哪裡獲得批准?
2023年11月,英國批准了人民的Casgevy超過12歲患有鐮狀細胞疾病或依賴輸血的β-甲性疾病。 12月,FDA批准了針對12歲及12歲以上患有鐮狀疾病的人的治療,並於2024年1月批准了Casgevy屬於依賴同一年齡類別的依賴輸血依賴性β-丘腦的人。
根據頂點,目前,歐盟的歐洲藥品局和沙特食品和藥品管理局正在審查這種待遇,因此其他國家可能很快批准了Casgevy。

Casgevy什麼時候可以為患者使用?
目前尚不清楚Casgevy何時可以使用,但其影響力很大程度上取決於其成本。基因療法可能會花費數百萬美元看來Casgevy也不例外。對於許多需要它的人來說,這可能使它無法訪問。
“挑戰在於,這些療法將非常昂貴,因此使這些療法在全球範圍內更容易獲得是關鍵,”凱·戴維斯(Kay Davies)牛津大學解剖學教授告訴英國科學媒體中心。
Vertex尚未為英國的Casgevy設定代價,該公司的發言人告訴大自然,但正在“與衛生當局合作,以確保盡快獲得合格患者的報銷和訪問權限”。
開發哪些其他CRISPR療法?
Intellia Therapeutics據STAT新聞報導,正在開發CRISPR療法以治療體內的遺傳疾病。
此外,調整了CRISPR版本,稱為“基礎編輯”,可以針對單個的構件脫氧核糖核酸正在測試是治療疾病的一種方式。例如,Verve Therapeutics正在測試這樣的心髒病實驗治療。另一種有希望的新型療法,稱為“主要編輯據STAT News報導,“涉及CRISPR但也涉及”其他酶和遺傳說明,以插入,刪除或重寫DNA的短片段。 ”
本文僅是出於信息目的,不打算提供醫療建議。
編者註:這個故事是最後一次更新於2024年1月18日更新,以反映FDA對Casgevy beta thalalsassia的認可。該文章於2023年11月22日首次發表,此前於12月8日更新。
曾經想知道為什麼有些人比其他人更容易建立肌肉或者為什麼雀斑在陽光下出來?向我們發送有關人體如何工作的問題[email protected]有了主題行“ Health Desk Q”,您可能會在網站上看到回答的問題!









