(半点图像/时刻/盖蒂图片社)
(半点图像/时刻/盖蒂图片社)
我们距离减少全天候注射胰岛素的需求又近了一步一项新的研究表明胰腺中产生胰岛素的细胞如何再生。
这一突破是通过让胰腺导管祖细胞(产生胰腺导管内层组织)发育来模仿胰腺的功能而取得的。β细胞1 型患者通常无效或缺失。
由澳大利亚贝克心脏和糖尿病研究所的一个团队领导的研究人员,研究了 FDA 已批准的针对糖尿病的药物的新用途。EZH2酶在人体组织中。通常,这种酶控制细胞发育,为生长提供重要的生物学检查。
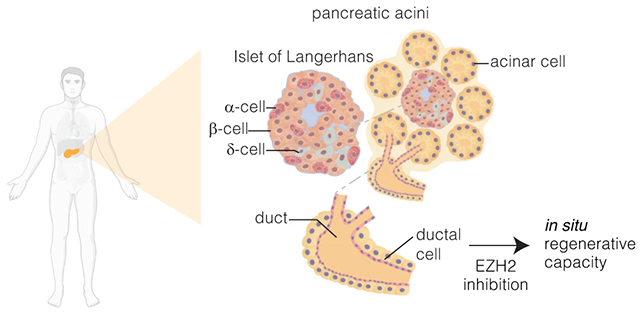
在这里,两种小分子抑制剂 GSK126 和 Tazemetostat 已被批准用于– 用于解除 EZH2 施加的一些制动,使导管祖细胞能够发展出与 β 细胞类似的功能。
研究人员在他们的论文中写道:“针对 EZH2 是 β 细胞再生潜力的基础。”发表论文。 “重新编程的胰腺导管细胞表现出胰岛素的产生和分泌,以响应离体的生理葡萄糖挑战。”
先前的研究研究表明,产生导管内壁的细胞(也有助于控制胃酸度)可以在适当的环境中转化为类似β细胞的细胞。现在,我们已经知道如何去做了。
至关重要的是,新细胞可以感知葡萄糖水平并相应地调整胰岛素的产生——就像β细胞一样。在该研究重点关注的1型糖尿病中,原始的β细胞被人体的免疫系统错误地破坏,这意味着血糖和胰岛素会下降定期注射。
研究小组进行的测试显示,取自两名年龄分别为 7 岁和 61 岁的 1 型糖尿病患者以及一名 56 岁的非糖尿病患者的组织样本中出现了相同的反应,这表明它可以跨代发挥作用。另一个积极的迹象是,只需要 48 小时的刺激就可以进行常规的刺激。恢复。
大约4.22 亿人全世界范围内都被认为患有糖尿病,依靠手动检查和管理血糖水平。这项研究还处于早期阶段虽然尚未到来,但这是诱导人体替代糖尿病所夺走的功能的另一种潜在方法。
这也不是科学家正在探索的唯一有希望的途径。正在开发中,同时研究人员也在研究方法在原始的胰岛素产生细胞被消灭之前
“我们认为这种再生方法是临床开发的重要进步,”说来自贝克心脏和糖尿病研究所的表观遗传学家 Sam El-Osta。
“到目前为止,再生过程一直是偶然的,并且缺乏证实,更重要的是,人类对控制这种再生的表观遗传机制仍然知之甚少。”
该研究发表于信号转导与靶向治疗。