與現有方法相比,一種新的細胞基因工程方法有望顯著提高速度、效率並減少細胞毒性。 賓州大學佩雷爾曼醫學院研究人員的一項研究表明,這種方法還可以推動癌症和其他疾病的先進細胞療法的開發。
在本週發表的這項研究中自然生物科技,研究人員發現一些病毒用來幫助它們進入細胞的技術也可用於將 CRISPR-Cas 基因編輯分子引入細胞及其含有 DNA 的細胞核,具有極高的效率和低細胞毒性。
科學家們預計這項新技術對於改造患者自身的 T 細胞和其他細胞以進行細胞療法特別有用。 其中一種應用可能是 CAR T(嵌合抗原受體 T 細胞)療法,它使用經過特殊修飾的來自患者以治療癌症。 T 細胞(一種白血球)從患者體內取出,並重新編程,以便在重新引入血液時發現並攻擊癌細胞。
第一個 FDA 批准的 CAR T 療法是由 Penn Medicine 開發的,並於 2017 年獲得美國食品和藥物管理局的批准。 這些療法徹底改變了某些 B 細胞白血病、淋巴瘤和其他血癌的治療方法,使許多原本沒有希望的患者獲得了長期緩解。
「這種新方法建立在 Penn Medicine 細胞和基因治療創新歷史的基礎上,有潛力成為工程細胞療法的主要支持技術,」共同高級作者 E. John Wherry 博士、Richard 和 Barbara 說。系統藥理學和轉化治療學主席傑出教授兼主席。
CRISPR-Cas 分子源自於古老的細菌抗病毒防禦,旨在精確去除細胞基因組中所需位置的 DNA。 一些基於 CRISPR-Cas 的系統將舊 DNA 的刪除與新 DNA 的插入結合起來,以進行多功能基因組編輯。 這種方法可用於用正確的基因替換有缺陷的基因,或刪除或修改基因以增強細胞功能。 一些系統還可以添加賦予 CAR T 細胞新特性的基因,例如識別腫瘤或承受通常會耗盡 T 細胞的惡劣腫瘤微環境的能力。
儘管 CRISPR-Cas 系統已經廣泛用作分子生物學的標準實驗室工具,但它們在修改患者細胞以進行基於細胞的療法方面的用途受到限制,部分原因是 CRISPR-Cas 分子很難進入細胞,然後進入含有DNA 的細胞核。
「目前將CRISPR-Cas 系統引入細胞的方法,包括使用載體病毒和電脈衝,對於直接取自患者的細胞(稱為原代細胞)來說效率低下。這些方法通常還會殺死許多使用它們的細胞。博士說。
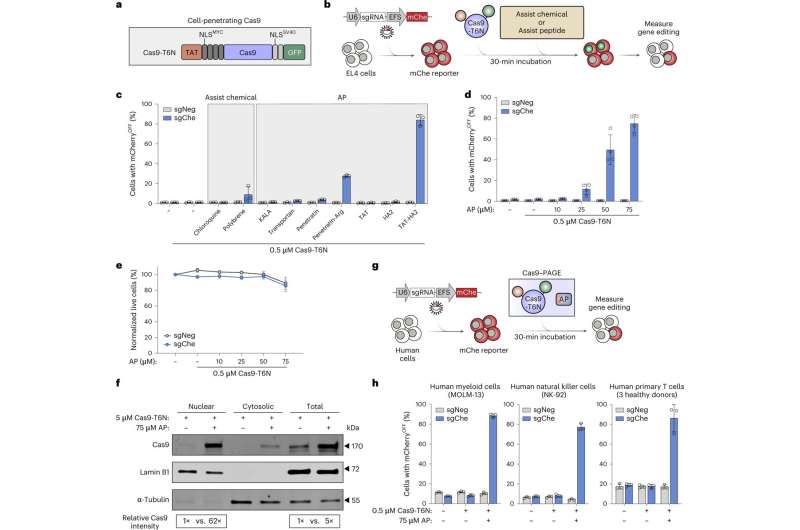
在這項研究中,研究人員探索了使用病毒衍生的小蛋白質片段(稱為勝肽)來更有效地引導 CRISPR-Cas 分子穿過原代人類細胞的外膜並進入細胞核。 值得注意的是,研究人員發現兩種修飾勝肽的融合組合——一種在 HIV 中發現,另一種在— 可與 CRISPR-Cas 分子混合,使它們進入原代人類或小鼠細胞及其細胞核,效率高達近 100%,具體取決於細胞類型 — 幾乎沒有毒性或基因表現變化。
團隊展示了這種被他們稱為 PAGE(勝肽輔助基因組編輯)的方法,適用於多種類型的設想細胞療法,包括 CAR T。
作者指出,除了在細胞和基因治療中的潛在用途外,PAGE 方法還可以在基礎科學研究中廣泛應用。 標準 CRISPR-Cas 細胞滲透方法效率低下,這意味著透過基因編輯創建小鼠疾病模型通常需要一個多步驟、耗時的過程來生成——將基因編輯機制引入他們的 DNA 中。 相較之下,PAGE 以其高效率和低毒性可能使普通實驗室小鼠的基因編輯快速、高效、簡單。
「勝肽輔助概念的簡單性和強大性表明,它在未來有可能適用於將其他基因組編輯蛋白,甚至基於蛋白質的藥物傳遞到原代細胞中,」共同高級作者史俊偉說,博士,癌症生物學助理教授,賓州大學表觀遺傳學研究所和艾布拉姆森家族癌症研究所成員。
這項研究是一項合作,包括賓州大學傳染病、生物化學和生物物理學副教授 Rahul Kohli 博士(醫學博士、博士)和合著者 Gerd Blobel 博士(醫學博士、博士)的實驗室。兒科教授兼表觀遺傳學研究所共同主任。
引文:改進的基因編輯方法可以為下一代細胞和基因療法提供動力(2023 年4 月28 日),2024 年6 月3 日檢索自https://webbedxp.com/science/jamaal/news/2023-04 -gene-method-power- Generation-cell.html
本文件受版權保護。 除私人學習或研究目的的公平交易外,未經書面許可不得複製任何部分。 內容僅供參考。









