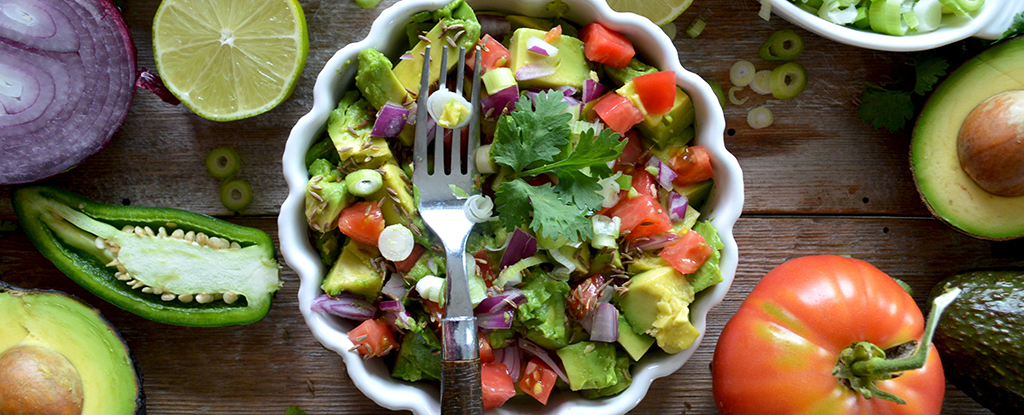对于生活在严重缺乏藻类食物的环境中的鱼类来说,苍白、无眼的粉红色墨西哥洞穴鱼却出人意料地胖乎乎的。
现在,一组研究人员已经弄清楚了这是怎么回事,它与导致人类胰岛素抵抗的机制相同。
胰岛素是胰腺产生的一种激素,有助于调节血液中的葡萄糖含量。 当您进食时,您的身体会将碳水化合物转化为葡萄糖,您的身体可以将其用作燃料。
胰岛素与肌肉、脂肪和肝细胞表面的受体结合,触发它们从血液中吸收葡萄糖。 这会使血糖水平恢复正常,并为您的身体提供能量,使用一些葡萄糖作为能量,并将多余的葡萄糖以糖原的形式储存起来供以后使用。
如果你一段时间不吃东西,血糖水平下降,胰腺就会释放第二种激素——胰高血糖素。 这会起到相反的作用,告诉肝脏和肌肉将糖原转化回葡萄糖并将其释放回血液中,从而恢复正常的血糖水平。
这种维持平衡的过程称为体内平衡。
有不同的形式糖尿病,但他们都阻止胰岛素正常发挥作用,导致血液中葡萄糖过多。 这对人类来说是危险的,但看起来一个物种的严重疾病是另一个物种的生存漏洞。
墨西哥四鱼(墨西哥阿斯蒂亚纳克斯)由两个不同的群体组成。 有居住在银灰色河流中的种群,可以接触到阳光照射的水域(和眼睛); 还有丰满的粉红色洞穴居民,他们在地球表面的黑暗中经历了长期的食物匮乏。
 (谜语等人/自然)
(谜语等人/自然)
此前曾观察到,当饥饿时,洞穴鱼体重减轻得多与居住在河流中的同种动物相比。 造成这种现象的因素有很多,包括代谢昼夜节律降低、代谢率降低和体脂升高,但这些背后的基因变化仍然是个谜。
在美国斯托尔斯医学研究所尼古拉斯·罗纳 (Nicolas Rohner) 的领导下,生物学家米斯蒂·里德尔 (Misty Riddle) 领导的一个研究小组现已确定,穴居鱼已经开发出一种突变版本的胰岛素受体,因此胰岛素无法结合。
他们在实验室中饲养了墨西哥阿斯蒂亚纳克斯(Astyanax Mexicanus)的河流和洞穴种群,并监测了它们的血糖。 他们发现,在进食和短期禁食后,洞穴鱼的血糖水平都高于河鱼。
然而,在长期禁食(21 天)后,洞穴鱼的血糖下降幅度比河鱼大得多。 这表明血糖稳态调节不良是洞穴鱼种群的特征。
为了研究潜在的遗传机制,研究人员检查了胰岛素途径中所有已知基因的序列,使用先前测序的基因组数据。 正是在那里,他们发现河鱼和洞穴鱼之间胰岛素受体基因的编码差异与胰岛素抵抗相关。
该突变导致氨基酸残基脯氨酸被亮氨酸取代。 这种基因改变与至少两例已知的罕见疾病有关拉布森-门登霍尔综合症,其特点是严重的胰岛素抵抗。
尽管高血糖和脂肪肝都与 2 型糖尿病有关,但到 14 岁时,洞穴鱼与生活在地表的表亲相比,表现出较少的衰老迹象。 生育能力下降也没有差异,这表明抵抗饥饿对生理健康的进化“成本”很小。
研究人员表示,这意味着它们可能还进化出了保持健康的补偿机制,尽管突变会对人类健康造成有害影响。 这些潜在的机制绝对值得进一步研究。
研究人员在论文中写道:“我们的研究结果将洞穴鱼作为一个模型,用于研究对类似糖尿病的葡萄糖稳态失调的病理学的抵抗力。”
“此外,我们的结果强调了极端的生理措施可以在关键的代谢途径中演变,以适应特殊的环境挑战。”