获奖图像揭示了阿尔茨海默氏症背后的隐藏罪魁祸首
一张图片的制作历时三个多月捕捉到小鼠脑肿瘤细胞相互作用的精确时刻,获胜第一名在尼康的第 50 个小世界显微摄影比赛。
奥古斯塔大学神经科学家 Bruno Cisterna 和细胞生物学家 Eric Vitriol 对细胞成分进行染色,揭示了支持和运输结构的破坏,这些破坏导致了神经退行性疾病,例如。
“神经退行性疾病的主要问题之一是我们不完全了解导致它们的原因,”解释水池。 “经过三年的研究,我们终于发表了我们的研究结果。”
这张照片揭示了两类细胞的微小细节:更圆、不太特化的类型和更长、更分化的神经元样细胞。如下图所示,细胞核被染成紫色,细胞骨架支撑结构被染成绿色。
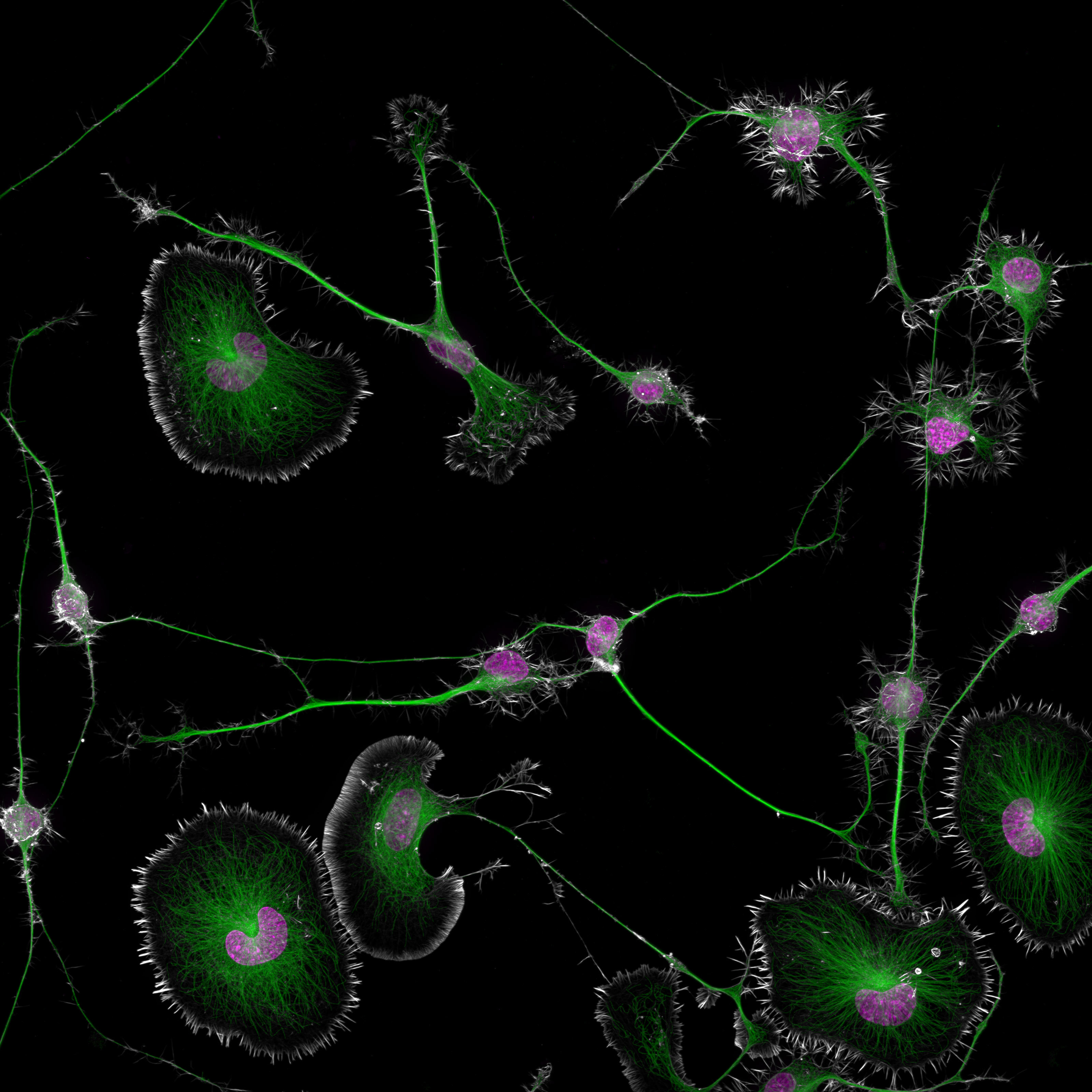
肌动蛋白和微管是细胞骨架的主要组成部分,它们不仅为细胞提供支撑支架,而且还充当运输其他细胞成分的运输系统。
Cisterna 和同事在显微镜下仔细观察两种不同细胞类型中的这些构建模块,意识到将两种细胞骨架成分连接在一起的蛋白质(称为 profilin 1 (PFN1))的破坏会导致运输系统受损,如图所示神经退行性疾病。
如果没有这种分子,线粒体和称为溶酶体的酶储存容器等细胞成分就会以比正常情况快得多的速度在细胞周围搅拌。这些变化在神经元样细胞类型中更为明显,其中的成分通过类似于神经细胞轴突的长分支运输。
“增强的轴突运输与 ALS 和阿尔茨海默病等神经退行性疾病有关,”Cisterna 和团队在他们的论文中解释。 “在这里,我们证明这也可能是 PFN1 功能丧失的结果。”
恢复正常的细胞骨架肌动蛋白和肌球蛋白水平使细胞能够再次正常运输其成分。这表明 PFN1 通过与复合物的肌动蛋白部分相互作用来调节转运系统。
“为了开发有效的治疗方法,我们需要首先弄清楚基础知识,”说坦克。
“我们的研究对于揭示这一知识并最终找到治疗方法至关重要。分化细胞可用于研究导致阿尔茨海默氏症或 ALS 的突变或有毒蛋白质如何改变神经元形态,以及筛选旨在保护神经元的潜在药物或基因疗法或恢复其功能。”
这些结果凸显了科学成像如何帮助揭示生物之谜。
“有时,我们忽视了周围世界的微小细节,”说尼康仪器高级经理埃里克·弗莱姆。 “尼康小世界提醒我们停下来,欣赏小事物的力量和美丽,并培养更深层次的探索和提问的好奇心。”
这项研究发表在细胞生物学杂志你可以看到一个整体这里还有其他微观奇迹的领域。