为了让人类在星际间冒险,我们必须解决一些严重的后勤问题。
其中最重要的是所涉及的旅行时间。太空如此之大,而人类的技术又如此有限,以至于前往另一颗恒星所需的时间构成了巨大的障碍。
例如,航行者一号探测器将需要73,000 年以目前的速度到达距离太阳最近的恒星比邻星。
Voyager 号在 40 多年前发射升空,预计更新的航天器可能会运行得更快;即便如此,以我们目前的技术来看,这一旅程仍然需要数千年的时间。
一种潜在的解决方案是一代飞船,它将见证多代太空旅行者在到达最终目的地之前生生死死。另一个方法是人工冬眠,如果它能够成功实施的话。
中国科学院深圳先进技术研究院(SIAT)的科学家们已经开始对此进行研究;不是在人类身上,而是在猴子身上,通过化学手段引发体温过低的状态。
“在这里,我们证明通过化学遗传学策略激活视前区(POA)神经元的亚群可以可靠地诱导麻醉和自由活动的猕猴体温过低,”研究人员在论文中写道。
“总而言之,我们的研究结果证明了灵长类动物体温的中枢调节,并为未来在临床实践中的应用铺平了道路。”
冬眠及其稍微不太昏迷的状态(麻木)是允许动物承受恶劣条件(例如极冷和低氧)的生理状态。
体温降低,新陈代谢减慢,使身体处于一种简单的“维持模式”——这是维持生命的最低限度。。
这种现象可以在多种动物身上发现,包括温血哺乳动物,但灵长类动物却很少。 SIAT的神经科学家王红和戴吉想看看他们是否可以通过化学操作下丘脑中负责睡眠和体温调节过程的神经元(视前神经元)来人为地诱导灵长类动物进入低代谢状态,甚至冬眠状态。
这项研究是在三只年轻的雄性食蟹猴身上进行的(食蟹猴)。在麻醉和非麻醉状态下,研究人员都使用了旨在激活大脑中特定修饰受体的药物,这些受体被称为“设计药物独家激活的设计受体”(Designer Receptors Exclusively Activated by Designer Drugs),或 DREADD。
然后,科学家们利用函数研究了结果、行为变化、生理生化变化。
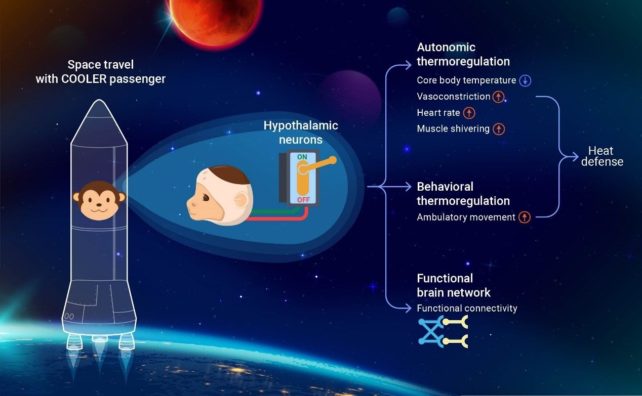
“为了研究视前区 (POA) 激活导致的全脑网络,我们进行了并确定了涉及温度调节和内感受的多个区域,”戴 说。
“这是第一项功能磁共振成像研究,旨在调查化学遗传学激活所揭示的全脑功能连接。”
研究人员发现一种名为氯氮平 N-氧化物的合成药物(中海油)在猕猴的麻醉和清醒状态下都能可靠地诱导体温过低。
然而,在麻醉的猴子中,CNO 引起的体温过低导致核心体温下降,从而阻止了外部加热。研究人员表示,这表明 POA 神经元在灵长类动物体温调节中发挥着关键作用。
研究人员记录了清醒猴子的行为变化,并将其与诱导低温小鼠的行为变化进行比较。通常,小鼠会减少活动,降低心率以试图保存热量。
相比之下,猴子的心率和活动水平有所增加,此外还开始发抖。这表明灵长类动物的体温调节比小鼠更复杂。人类的冬眠()需要考虑到这一点。
“这项工作首次成功证明了基于有针对性的神经元操纵的灵长类动物的体温过低,”王说。
“随着人类对太空飞行的热情日益高涨,这种低温猴模型是人工冬眠漫长道路上的一个里程碑。”
该研究发表于创新。